Schülerprotokoll
Aufgabe: Prüfen Sie
Glucose- und Fructoselösung (10%ig) mit Glucoseteststreifen!
Geräte: 3
Bechergläser
1 Rührstab
3 Glucoseteststreifen
1 elektronische Waage
Chemikalien: Wasser
Glucose
Fructose
Durchführung: Glucoselösung herstellen:
1 g
Glucose und 10 ml Wasser in einem Becherglas mit einem Rührstab vermischen
Fructoselösung herstellen:
1 g
Fructose und 10 ml Wasser in einem Becherglas mit einem Rührstab vermischen
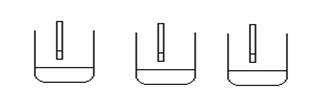
Teststreifen
10 ml 10%ige 10 ml 10%ige 10 ml Wasser
Glucoselösung Fructoselösung
Das kürzere weiße Ende unter dem
gelben Strich kurz in die Lösungen und das Wasser tauchen.
Nach zwei Minuten die Färbung mit
der Farbskala vergleichen
Beobachtung: Nur der
Teststreifen mit der Glucoselösung färbt sich grünlich.
Die Teststreifen mit der
Fructoselösung und dem Wasser bleiben gelb
Auswertung: Das Testpapier
enthält Verbindungen, die nur mit der Aldehydgruppe der Glucoselösung
reagieren, und einen Farbumschlag zu grün bewirken. Der Teststreifen
kann daher nicht mit
der
Fructoselösung und auch nicht mit Wasser reagieren da die beiden Stoffe die
benötigte
funktionelle Gruppe (Aldehydgruppe) nich aufweisen können. Fructose hat
zwar eine
funktionelle Gruppe aber die ist eine Keto-Gruppe.
Glucose ist ein Zucker der zu den Monosacchariden gehört und die
chemische Summenformel C6H12O6 hat. Die
Glucose kommt im Honig und im Saft vieler Früchte vor, so beispielsweise in den
Weintrauben; daher wird sie auch Traubenzucker genannt. Glucose lässt sich durch
Hydrolyse natürlicher Glycoside herstellen und ist z. B. im Blut
enthalten.
Glucose ist ein
weißer, kristalliner Feststoff und schmeckt weniger süß als Rübenzucker.
Bestrahlt man eine wässrige Glucoselösung mit polarisiertem Licht, so wird die
Polarisationsebene des Lichtes nach rechts gedreht. Diese Eigenschaft gab der
Glucose auch den Namen Dextrose (lateinisch dexter: rechts). Glucose kommt in
drei verschiedenen Molekülstrukturen vor, die die Polarisationsebene des
Lichtes unterschiedlich stark drehen.
Eine besondere
Eigenschaft, die man erstmals bei der Glucose beobachtete, ist die
Mutarotation. Durch dieses Phänomen ändert sich im Lauf der Zeit der optische
Drehwert (Drehung polarisierten Lichtes) einer wässrigen Glucoselösung. Diese
Anderung hängt mit der Umwandlung der einen Molekülstruktur in die andere
Struktur zusammen. In Lösung stellt sich nämlich zwischen den unterschiedlichen
Glucosestrukturen (so genannte Anomere) ein Gleichgewicht ein. Mutarotation
lässt sich auch bei anderen optisch aktiven Substanzen beobachten.
Glucose entsteht
bei der Hydrolyse vieler Kohlenhydrate, wie z. B. Saccharose, Maltose,
Cellulose, Stärke und Glykogen. Die Gärung der Glucose mit Hilfe von Hefe
erzeugt Ethylalkohol (auch Ethanol) und Kohlendioxid. Industriell produziert
man sie durch Hydrolyse von Stärke unter Einwirkung verdünnter Säure oder
(häufiger) von Enzymen. Glucose wird vor allem in der Nahrungsmittelindustrie
zum Süßen verwendet. Außerdem benötigt man sie beispielsweise zum Gerben, für
Färbebäder und in der Medizin zum Behandeln von Wasserverlust und zur
intravenösen Ernährung.
Fructose, auch Fruchtzucker genannt, ist ein Monosaccharid mit der Formel C6H12O6,
das zusammen mit Glucose in süßem Obst und in Fruchtsäften vorkommt. Fructose
entsteht wie Glucose durch die Spaltung von Saccharose sowie bei der Hydrolyse
verschiedener Kohlenhydrate; zur künstlichen Herstellung behandelt man am
besten das Kohlenhydrat Inulin mit verdünnter Säure. Fructose lässt sich nur
schwer kristallisieren. Die Kristalle schmelzen bei 102 bis 104 °C. Die
Verbindung ist linksdrehend, d. h. eine Fructoselösung dreht die Ebene
polarisierten Lichtes nach links. Hefe vergärt Fructose zu Ethanol und
Kohlendioxid.
Amylase kommt im Speichel der Mund- und der Bauchspeicheldrüse vor. Sie
spaltet die
Stärke zu Maltose, die dann zu Glucose aufgespalten wird. Enzyme sind
Biokatalysatoren,
das heißt sie sind Wirkstoffe, die vom Körper gebildet werden um
biochemische
Reaktionen zu beeinflussen. Sie sind Eiweißmoleküle, die einen Zusatz
wie ein Metallion
oder ein Vitamin haben können. Nach der Reaktion, liegt ein Enzym
wieder in
seinem ursprünglichen Zustand vor. Sie besitzen ein aktives Zentrum, an
dem die
Reaktionen statt finden. Dort
wird zum Beispiel auch die Stärke gespalten. Sie sind substrat-
und reaktionsspezifisch. Das bedeutet, dass sie nur mit den für sie
vorgesehenen Substraten
auf eine ganz bestimmte Art und Weise reagieren können. Bei einer
enzymatischen Spaltung
geht ein Substrat eine lockere Verbindung mit einem Enzym ein, wodurch
ein Enzym-
Substrat-Komplex entsteht. Nach der Reaktion am aktiven Zentrum liegt
das Enzym und ein
Produkt vor.
Schülerprotokoll Nr 7
Aufgabe: Weisen Sie Stärkelösung mit
Lugolscher Lösung nach! Führen Sie die hydrolytische Spaltung
mit einer Enzymlösung
(Amylase) durch!
Geräte: Reagenzgläser
Reagenzglasständer
Chemikalien: Stärkelösung
Iodkaliumiodidlösung (Lugolsche Lösung)
Amylase in Form von Speichel
Durchführung: 1. Stärkelösung in ein Reagenzglas geben
2. 2 - 3 Tropfen Lugolsche Lösung hinzugeben
3. Reagenzglas schütteln
4. Amylase in Form von Speichel hinzugeben
5. Reagenzglas erneut schütteln
Beobachtung: Nach Zugabe der
Iodkaliumiodidlösung entsteht eine tiefblaue Färbung.
Beim Hinzugeben der Amylase verschwindet
diese Verfärbung
Auswertung: Die Blaufärbung kommt zustande, weil sich
die Iodmoleküle in die Helixstruktur der Stärke
einlagern, deshalb
reflektiert die Iodstärkeverbindung die blauen Farbteile des Lichtes.
Bei der enzymatischen Spaltung wird die
Stärke in Maltose aufgespalten. Dadurch zerfällt die
Helixstruktur der Stärke und die Iodmoleküle werden freigesetzt und
dadurch verschwindet die
Blaufärbung. Es handelt sich hierbei um eine hydrolytische Spaltung, bei
der Wasser
aufgenommen wird.
Stärke ist die übliche Bezeichnung für ein komplex aufgebautes
Kohlenhydrat mit der allgemeinen chemischen Formel (C6H10O5)n.
In reinem Zustand ist Stärke eine weiße, körnige oder pulverige, geruch- und
geschmacklose Substanz. Sie kommt u. a. in den Samen von Getreidepflanzen
sowie in Pflanzenknollen und -zwiebeln vor. Stärkemoleküle enthalten Hunderte
oder Tausende von Atomen, d. h. die Zahl n in der obigen Formel liegt
zwischen 50 und vielen tausend.
Stärke kommt in
zwei Molekülformen vor. Die Amylose macht etwa 20 Prozent der gewöhnlichen
Stärke aus. In ihr sind die Glucosemoleküle (C6H10O5-Gruppen)
zu einer überwiegend unverzweigten Kette miteinander verbunden. Diese Kette
bildet eine spiralförmige Helix. Bei der anderen Form, dem Amylopectin, sind
zahlreiche, buschartige Kettenverzweigungen vorhanden. Hier sind die Ketten
kürzer und enthalten nur 20 bis 25 Glucoseeinheiten.
Stärke entsteht in
den Grünpflanzen durch Photosynthese und bildet in den Pflanzen einen Teil der
Zellwände und auch der steifen Fasern. Ferner dient sie den Pflanzen als eine
Art Energiespeicher, da ihre Oxidation zu Kohlendioxid und Wasser erhebliche
Energiemengen freisetzt. Die Form und Größe der Stärkekörnchen sind charakteristisch
für die Pflanze, in der die betreffende Stärke entstand.
Stärke ist in
kaltem Wasser und in Alkohol fast unlöslich. In kochendem Wasser bildet sich
Stärkekleister, der beim Abkühlen zu einer Gallerte werden kann. In heißem
Wasser geht die Amylose kolloidal* in Lösung. Sie lässt sich aus dem Filtrat
mit Alkohol als lösliche Stärke isolieren. Durch Kochen mit verdünnter Säure
wandelt sich die Stärke allmählich in Dextrine um, die aus kleineren Molekülen
bestehen. Diese Reaktion ist ein Beispiel für eine Hydrolyse wird
beispielsweise auch durch einige Enzyme katalysiert. Dextrine werden u. a.
als Klebstoffe und Appreturmittel verwendet. Der gezielte Abbau von Stärke ist
auf enzymatischem Weg möglich. Letztlich entsteht dabei das Disaccharid Maltose
(Malzzucker, C12H22O11) und das Monosaccharid
Glucose (Traubenzucker, C6H 12O6).
Bei der Verdauung
der Stärke im menschlichen Körper beginnt die Hydrolyse bereits im Mund durch
die Einwirkung des Ptyalins im Speichel. Der Körper verbraucht nicht sofort die
gesamte bei der Stärkeverdauung entstandene Menge an Glucose, sondern wandelt
den größten Teil in Glycogen um, das in der Leber gespeichert wird. Glycogen,
auch tierische Stärke genannt, hat eine Struktur, die mit der des Amylopectins
nahezu identisch ist. Wenn der Körper später Glucose benötigt, dann wird
Glycogen hydrolysiert und dem Blutstrom zugeführt. Somit stellt das Glycogen
bei Mensch und Tier eine Energiereserve dar, ähnlich wie die Stärke bei den
Pflanzen.
*äusserst fein verteilte Partikel in einer Flüssigkeit oder in einem
anderen Stoff
Aufgabe: Überprüfen Sie
verschiedene gegebene Materialien auf Vorhandensein von Cellulose, indem
einige
Tropfen Chlorzinklösung hinzu gegeben werden.
Geräte: 4 Schalen
Chemikalien: Chlorzinklösung
Filterpapier
Ein Stück Baumwollstoff
Papier
Zellstofftaschentuch
Durchführung: Chlorzinklösung wird auf die zu erprobenden Materialien
geträufelt.
Beobachtung: Die getesteten
Stoffe weisen eine rot-violette Färbung auf.
Auswertung: Durch die
rot-violett Färbung wird Cellulose nachgewiesen, die in den Zellwänden der
Pflanzen
vorhanden ist.
Cellulose (lateinisch cellula: kleine Zelle), komplexe aus Glucoseeinheiten
aufgebaute Kohlenhydratverbindung, die Hauptbestandteil der Zellwände von
Pflanzenzellen ist. Mit Ausnahme der Manteltiere ist Cellulose in tierischen
Geweben nicht zu finden. In den Verdauungssystemen Pflanzen fressender Tiere
wird Cellulose biologisch durch Mikroorganismen, die Cellulose abbauende Enzyme
besitzen, in verwertbare Produkte bis zur Glucose gespalten. Cellulose ist in
Wasser und organischen Lösungsmitteln unlöslich und kann daher leicht von anderen
Bestandteilen der Pflanzen getrennt werden. Cellulose ist von großer
technischer und wirtschaftlicher Bedeutung. Chemisch wird Cellulose durch
Säuren hydrolytisch gespalten. Bei der Verwendung konzentrierter Säure,
beispielsweise konzentrierter Schwefelsäure, kann der Abbau bis zur Glucose
erfolgen und ist damit industriell für die Holzverzuckerung von Bedeutung. Bei
diesem Vorgang kann auch lösliche Stärke oder Amyloid, ein Stärkederivat,
entstehen. Wird Cellulose mit Alkalien behandelt und anschließend Kohlendisulfiddämpfen
ausgesetzt, entstehen daraus u. a. Chemiefasern und Folien. Reyon und
Cellophan werden beispielsweise aus einer solchen Lösung regeneriert.
Celluloseacetate werden zur Herstellung von Fasern, Folien, photographischen
Filmen, Glasersatz und Lackbindemitteln verwendet. Celluloseether finden in
Papierleim, Klebstoffen, Seifen und synthetischen Harzen breite Anwendung.
Durch Veresterung von Cellulose mit Salpetersäure
und Schwefelsäure entstehen verschiedene brennbare, explosive Verbindungen, die
als Nitrocellulosen, richtiger Cellulosenitrate, bekannt sind. Je nach
Stickstoffgehalt unterscheidet man mehrere Cellulosenitrate: Kollodiumwolle
wird als Bindemittel für Lacke und zur Herstellung von Celluloid verwendet. Die
Schießwolle mit einem geringfügig höheren Stickstoffgehalt dient für
Explosivstoffe.