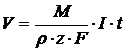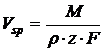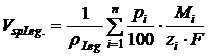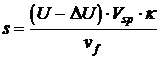Elektrochemisches Abtragen
Das elektrochemische Abtragen beruht auf der Auflösung eines als Anode
(positiv) polarisierten metallischen Werkstoffs in einem elektrisch leitenden
Medium. Der dazu erforderliche Stromfluß kann durch eine äußere, aber auch
durch eine innere Spannungsquelle hervorgerufen werden.
Prinzip der anodischen Metallauflösung
Die Grundlage der anodischen Metallauflösung mit Hilfe einer äußeren
Spannungsquelle ist in folgendem Bild dargestellt.(Bild4-1)
Der positive Pol einer Gleichspannungsquelle wird an den abzutragenden
metallischen Werkstoff (Anode ) gelegt, der negative Pol an eine ebenfalls
metallische Kathode. Für den Stromtransport zwischen diesen beiden Elektroden
ist weiterhin ein elektrisch leitendes Medium erforderlich, in der Regel werden
dazu wäßrige Natriumnitrat- oder Natriumchlorid-Elektrolytlösungen eingesetzt.
In Sonderfällen kommen auch saure bzw. basische Lösungen zum Einsatz.
Durch das Anlegen der Gleichspannung laufen an den Elektroden komplexe
elektrochemische Reaktionen ab. An der Anode geht das abzutragende Metall unter
Abgabe von Elektronen als Metallionen in die Elektrolytlösung über. He nach den
chemischen Eigenschaften der Metallionen entweder gelöst, oder reagieren mit
Bestandteilen der Elektrolytlösung, z.B. unter Bildung von Metallhydroxiden.
Diese sind in der Elektrolytlösung nicht löslich und fallen aus, wodurch ein
Entfernen der Abtragprodukte (als Hydroxide) mit Hilfe einfacher Trennverfahren
(Absetzbehälter, Zentrifuge, Filterpresse) möglich ist.
An der Kathode laufen ebenfalls elektrochemische Reaktionen ab, an denen die
Bestandteile der Eletkrolytlösung beteiligt sind. An der Kathode erfolgt
allerdings kein Abtrag.
Der Werkstoffabtrag an der Anode wird durch das Faradaysche Gesetz beschrieben,
nach dem die anodenseitig abgetragene Masse m proportional zu Molmasse M des
aufgelösten Materials und zur geflossenen Ladungsmenge I*t ist. Die
mathematische Formulierung dieses Zusammenhangs lautet wie folgt:
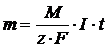
m abgetragene Masse in g
M Molmasse in g/mol
I Stromstärke in A
t Bearbeitungszeit in s
z elektrochemische Wertigkeitsänderung
(z.B. für die Reaktion 
F Faradaykonstante (96487 A*s/mol)
Unter Berücksichtigung der Dichte 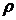 berechnet sich das
aufgelöste Materialvolumen V zu:
berechnet sich das
aufgelöste Materialvolumen V zu:
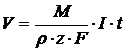
Der das aufgelöste Materialvolumen V und die transportierte Ladungsmenge I*t
verknüpfende Proportionalitätsfaktor , das spezifische Abtragvolumen
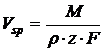
ist für eine bekannte Reaktion eine Materialkonstante, falls die
elektrochemische Wertigkeitsänderung z konstant bleibt. Die Bearbeitbarkeit
eines Werkstoffs hängt deshalb nur von seinen elektrochemischen Eigenschaften
bzw. von dessen Reaktionsprodukten ab, nicht aber von den mechanischen
Eigenschaften, wie z.B. der Zugfestigkeit.
Besteht ein Werkstoff aus mehreren Legierungselementen 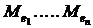 mit den
Massenprozentanteilen
mit den
Massenprozentanteilen  und den Molmassen
und den Molmassen  , so läßt sich ebenfalls das spezifische Abtragvolumen der
Legierung
, so läßt sich ebenfalls das spezifische Abtragvolumen der
Legierung 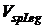 durch Superposition
der Einzelkomponentenabträge berechnen:
durch Superposition
der Einzelkomponentenabträge berechnen:
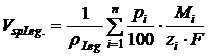
Dieser theoretische Zusammenhang gilt jedoch nur für die Bedingung, daß
ausschließlich die in diesem Ansatz vorausgesetzten Reaktionen mit den
eingesetzten elektrochemischen Wertigkeitsänderungen zi ablaufen.
Passivität
Eine weitere Voraussetzung für die Anwendbarkeit des Faradayschen Gesetztes
ist, daß die gesamte dem Prozeß zugeführte Ladungsmenge für abtragwirksame
Reaktionen verbraucht wird. Im Verlauf des elektrochemischen Prozesses wird
aber die Geschwindigkeit des metallischen Auflösevorgangs von den Gesetzen der
elektrochemischen Kinetik bestimmt. Der bestimmende Faktor ist dabei das
Elektrodenpotential. Bei bestimmten Elektrodenpotentialen werden auch die Ionen
des wäßrigen Elektrolyten oxidiert bzw. reduziert, so daß an der Anode (dem,
Werkstück) Sauerstoff entsteht bzw. an der Kathode (dem Werkzeug) Wasserstoff
entwickelt wird. Ebenfalls können bereits aufgelöste Metallionen oxidiert oder
reduziert werden. Bei der Verwendung von Natriumnitrat - Elektrolyten werden
die Nitrationen teilweise zu niedrigeren Oxidationsstufen des Stickstoffs
reduziert (Nitrit, Hydroxylamin und Ammonium). Somit wird ein Teil der
zugeführten elektrischen Energie für abtragunwirksame Reaktionen verbraucht,
wodurch der Wirkungsgrad der anodischen Metallauflösung verringert wird.
Außer den angeführten Redox- Reaktionen bildet sich bei bestimmten
Elektroden-potentialen auf der Anodenoberfläche eine Oxidschicht aus. Diese
behindert den Übergang der Metallionen in die Elektrolytlösung. Die Ausbildung
solcher Deckschichten, auch Passivschichten genannt, wird zudem von der Art des
Elektrolyten und den vorliegenden Elektrolysebedingungen sowie von dem
Anodenwerkstoff selbst beeinflußt. Letzterem kommt dabei besondere Bedeutung
zu.
Dieses bisher in der Elektorchemie häufig untersuchte Phänomen, das zum ersten
Mal an Eisen und später auch an anderen Metallen beobachtet wurde, ist im
Schrifttum unter dem Begriff Passivität bekannt. Durch die Annahme einer
Stromdichte-Potential-Kennlinie kann die Passivität meßtechnisch erfaßt werden.
(Bild 4-3)
Nach einer mit zunehmendem Anodenpotential zunächst ansteigenden Stromdichte
sinkt diese nach Erreichen einer Potentialschwelle, die nach ihrem Entdecker
"Flade-Potential" genannt wird, auf den Betrag der "Korrosoinsstromdichte" ab.
Ein erneutes Ansteigen der Stromdichte wird erst bei höheren Anodenpotentialen
beobachtet, bei denen die Auflösung dann transpassiv einsetzt.
Im passiven Bereich wirken sich nach einer Deckschichtbildung die
elektro-chemischen Eigenschaften der Metalloxidoberfläche auf den Metallabtrag
aus. Dieser wird vernehmlich durch die Struktur, die Porosität und die
Leitfähigkeit der Deckschicht für die Ladungsträger und die chemische
Löslichkeit der Oxide beeinflußt.
In bestimmten Anwendungsfällen ist die Ausbildung von Passivschichten
erwünscht, da sie die Erzeugung einer guten Oberflächenqualität ermöglicht.
Die angeführten abtragunwirksamen Reaktionen, welche das Passivitätsverhalten
und die ablaufenden Redox-Reaktionen bestimmen, sind potential- und damit auch
stromdichteabhängig, so daß das aus den theoretischen Zusammenhängen des
Faradayschen Gesetzes hergeleitete spezifische Abtragvolumen Vsp
nicht immer die Eigenschaft eines konstanten Proportionalitätsfaktors hat;
vielmehr ist dieser Kennwert auch mit der Stromdichte veränderlich. Dieser
veränderliche, den tatsächlichen Zusammenhang zwischen dem aufgelösten
Materialvolumen und der am Umsatz beteiligten Ladung beschreibende Faktor wird
als "effektives Abtragvolumen" Veff bezeichnet. Diese Kenngröße ist
mit dem Wirkungsgrad verknüpft, der die während des elektrochemischen
Prozeßablaufs auftretenden Abweichungen der elektrochemischen
Wertigkeitsänderung und die Energie-verluste durch abtragunwirksame Reaktionen
berücksichtigt:
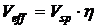
Hiernach ist das effektive Abtragvolumen proportional dem Wirkungsgrad  und hat mithin die
gleiche Aussagekraft wie die "Stromausbeute"
und hat mithin die
gleiche Aussagekraft wie die "Stromausbeute"
Auswahl der Elektrolyte
Die Elektrolytlösung hat bei der Elektrolyse die Funktion, die in der Lösung
vorhandenen Ladungsträger zu transportieren und an den Elektroden eine elektrochemische
Umsetzung hervorzurufen. Weitere Anforderungen, die zusätzlich an die
Elektrolytlösung gestellt werden müssen, sind
hohe
chemische Stabilität, das heißt, daß die Elektrolytlösung eine dauerhafte Erhaltung
ihrer Eigenschaften zeigen soll
geringe
Korrosionswirkung auf die Bearbeitungsapparatur
physiologische
Neutralität in bezug auf das Bedienungspersonal
Preisgünstigkeit
Aufgrund der unterschiedlichen Bedingungen, denen eine Elektrolytlösung genügen
muß, kann man keine eindeutigen Aussagen über den im Einzelfall anzuwendenden
Elektrolyten machen.
Die Leitfähigkeit einer Elektrolytlösung ist direkt abhängig von
der
Art und der Zusammensetzung des Elektroylten
der
Konzentration und der Temperatur
der
kathodisch entwickelten Wasserstoffmenge
der
Art der Abtragungsprodukte
Für gebräuchliche Elektrolytlösungen (NaCl und NaNO3) liegt die
spezifische Leitfähigkeit zwischen 5 und 30 S/m.
In der Praxis kommen vorwiegend folgende Elektrolytlösungen mit
unterschiedlichen Konzentrationen und Temperaturbereichen zum Einsatz:
Kochsalzlösungen (NaCl)
Bei Bearbeitungsprozessen mit
Natriumchloridlösungen kommt es wegen der
großen Adsorptionsaffinität der Chloridionen zu einer vorrangigen Adsorption dieser Ionen auf der
Metalloberfläche im Vergleich zu den OH-- Ionen oder den Wasserdipolen. Dadurch können die
Metallionen direkt mit den
Chloridionen reagieren. Meist bildet sich dabei das lösliche Metall- chlorid. In einem anschließenden
Hydrolysevorgang werden die Chlorid- ionen
durch OH--Ionen ausgetauscht und es entsteht das in der Elektrolyt- lösung ausfallende Metallhydroxid. Wegen der
bei hohn Stromdichten auftretenden großen
Bildungsgeschindigkeit der Metallchloride wird deren Sättingungsgrenze in der Elektrolytlösung überschritten.
Dies führt zur Bildung eines viskosen
Elektrolytfilms in Anodennähe, der eine Einebnung der Oberfläche bewirkt. Weiterhin zeichnen sich diese
Elektrolyte bei der Bearbeitung der
meisten Stähle durch hohe Stromausbeuten aus; ein Materialabtrag findet schon im unteren Potentialbereich
statt
Nitratlösungen (NaNo3)
Im Gegensatz zu den
Kochsalzlösungen verläuft die Metallauflösung bei der Verwendung von Natriumnitratlösungen über einen
Oxidationsvorgang des Metalls
im sogenannten transpassiven Bereich. Dabei wird in einer Nebenreaktion die bei der Bearbeitung
von Kohlenstoffstählen erwünschte Passivschicht
ausgebildet, welche zu einer guten Abbildungsgenauigkeit führt.
Arbeitet man im unteren
Stromdichtebereich, so wird nur wenig Metall aufgelöst,
da nahezu die gesamte Ladungsmenge für die Sauerstoff- entwicklung verbraucht wird.
Säuren
Während bei den bisher genannten
Elektrolytlösungen die Anodenreaktionsprodukte
in der Regel als Metallhydroxide ausgefällt werden,
bleiben die Abtragprodukte beim Einsatz von starken Säuren (H2SO4, HNO3,
HCl) in dem jeweils verwendeten Arbeitsmedium gelöst.
Um eine bei dieser Arbeitsweise
mögliche Abscheidung der Metallionen auf den
Kathoden in erträglichen Grenzen zu halten, kann der Elektrolyt nur jeweils so lange verwendet werden, bis eine
bestimmte maximale Metall- ionenkonzentration
erreicht ist. Dann muß man den Elektrolyten erneuern oder in einem Ionenaustauscher aufarbeiten. Ebenfalls muß der
pH-Wert durch stetige Zugabe von Säure
geregelt werden.
Die Anwendung ist wegen der
hohen Aggressivität der Säuren auf Sonderfälle
beschränkt.
Weiterhin kommen auch Mischungen der beschriebenen Elektrolyte zum Einsatz;
außerdem werden auch je nach Bearbeitungsaufgabe Komplexbildner (Citrate =
Salze der Citronensäure und Tartrate = Salze der Weinsäure) verwendet.
Elektrochemisches Senken
In der Regel wird das katodisch gepolte Bearbeitungswerkzeug
(Werkzeug-elektrode) mit konstanter Vorschubgeschwindigkeit in das anodisch
gepolte Werkstück (Werkstückelektrode) eingesentk. Zwischen Werkstück und
Werkzeug bildet sich prozeßbedingt ein Arbeitspalt aus, durch den die
Elektrolytlösung mit hoher Geschwindigkeit strömt und dabei die im Arbeitsspalt
entstehenden Abtrag-produkte sowie durch den Stromfluß entstehende Joulesche
Wärme abführt.
Zwischen Werkzeug und Werkstück bildet sich verfahrensbedingt ein Spalt aus, so
daß streng genommen nicht von einer direkten Abbildung des Werkzeuges im
Werkstück gesprochen werden kann. Vielmehr unterschiedet sich die Werkstück-geometrie
von der Werkzeuggeometrie um den Betrag des Arbeitsspalts. Zur Her-stellung
eines maßgenauen Werkstücks muß deshalb das Werkzeug um diesen betrag
berichtigt werden; dies setzt die Kenntnis der Spaltausbildung voraus.
In erster Näherung kann die Spaltausbildung mit Hilfe des Ohmschen und des
Faradayschen Gesetzes berechnet werden.(Bild4-4)
Der Spannungsabfall in der Elektrolytlösung Uel berechnet sich zu
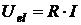
wobei der Widerstand der Elektrolytlösung R von der spezifischen Leitfähigkeit 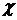 der Spaltweite s und
der Elektrodenfläche A abhängig ist.
der Spaltweite s und
der Elektrodenfläche A abhängig ist.
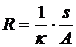
Berücksichtigt man, daß die Stromdichte J
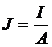
ist, so ergibt sich für die Spaltweite s

Die anzulegende Arbeitsspannung U setzt sich aus dem Spannungsabfall in der
Elektrolytlösung Uel und der anodischen (UpolAn) sowie
der kathodischen (UpolKa) Polarisationsspannung zusammen:
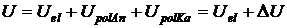
Das aufgelöste Materialvolumen V kann aus der Abtraggeschwindigkeit vA,
der Elektrodenfläche A und der Bearbeitungszeit t berechnet werden:
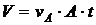
Nach dem Faradayschen Gesetz ist dieses Volumen von dem spezifischen
Abtragvolumen Vsp abhängig:
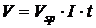
Durch Kombination dieser Gleichungen erhält man unter Berücksichtigung der
Stromdichte J die Abbtraggeschwindigkeit vA:

Im Falle stationärer Senkbedingungen ist die Abtraggeschwindigkeit vA
gleich der Vorschubgeschwindigkeit vf.
Unter Berücksichtigung dieser Zusammenhänge berechnet sich die Spaltweite nun
folgendermaßen:
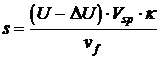
Die Spaltweite s ist damit von den Einstellparametern Arbeitspannung U und
Vorschubgeschwindigkeit vf sei den werkstoffspezifischen Kenngrößen
spezi-fisches Abtragvolumen Vsp und Polarisationsspannung DU abhängig. Außerdem ist sie direkt proporional zur
spezifischen Leitfähigkeit k des
Elektrolyten, welche von dessen Zusammensetzung, Konzentration und Temperatur
bestimmt wird. Darüber hinaus ergibt sich, daß die Spaltweite s und die
Stromdichte j umgekehrt proportional sind:

Entsprechend dem Zusammenhang zwischen der Abtraggeschwindigkeit vA
und der Stromdichte J bedingen unterschiedlich vorgegebene
Vorschubgeschwindig-keiten vf unterschieldiche Stromdichten J.
Daraus entstehen wiederum unterschiedliche Spaltenweiten s.(Bild 4-5)
Die Abtraggeschwindigkeit vA läßt sich direkt aus der
Vorschubgeschwindigkeit vf der Werkzeugelektrode schon während des
elektrochemischen Bearbeitungs-prozesses ablesen. Prozeßbedingt wird sich
bereits nach kurzer Zeit ein stationärer Gleichgewichtszustand einstellen, bei
dem sich ein konstanter Arbeitsspalt s mit einer konstanten Stromdichte J boldet
. Stationäre Bedingunge werden damit während der Bearbeitung an der Konstanz
der Stromdichte erkannt. Die Abtraggeschwindigkeit entspricht dann der
bekannten vorgegebenen Vorschubgeschwindigkeit und sit somit erfa´bar.
Unter Polarisationsspannung DU wird
der Spannungsabfall an den Phasengrenzen Elektroden/Elektrolytlösung verstanden. Wird die Spaltweite s in
Abhängigkeit von der an die Elektroden angelegten Arbeitsspannung U für
unterschiedliche Leitfähigkeiten k oder
auch Vorschubgeschwindigkeiten vf gemessen, ergeben sich Geraden,
die nicht durch den Koordiantenursprung laufen, sondern die Aszisse um den
Betrag der Polarisationsspannung DU
versetzt schneiden.
Dies bedeutet, daß sich erst dann eine endliche Spaltweite s ausbilden kann,
wenn zwischen den Elektroden eine Spannung angelegt wird, die größer als die
Polarisationsspannung DU ist.
Beim Einsenken von Raumformen wird die Spaltausbildung von einer weiteren
Variablen, und zwar vom Neigungswinkel der Werkstückkontur, bestimmt.(bild
4-6)
Wie aus obigem Bild zu entnehmen ist, änder sich die Normalkomponente der
Abtraggeschwindigkeit mit dem Sinus des Konturneigungswinkels a. Setzt man diese Normalkomponente an Stelle der
Vorschubgeschwindigkeit vf in die Gleichung für die Spaltweite s ein, so ergibt
sich ein um so größerer Spalt, je steiler die Kontur ist.
Bei zylindrischen Formen oder Durchbrüchen (zweidimensionale Geometrie) ist
eine Korrektur der Werkzeugelektrode verhältnismäßig einfach, da sich hier bei
der Isolierung der Werkzeugseitenwände ein nahezu konstanter Seitenspalt
ausbildet. Die Werkzeugkorrektur erreicht man dabei durch eine allseitige
Verkleinerung um den Betrag des Seitenspalts, der in empirischen Untersuchungen
in Abhängigkeit von den Bearbeitungsbedingungen und der Werkzeuggeometrie
bestimmt wird. Je nach Korrekturaufwand sind Genauigkeiten von bis zu 0,01mm
erreichbar.
Bei dreidimensionalen Raumformen ist eine Werkzeugkorrektur nicht mehr so
einfach auszuführen, weil der Korrekturbetrag aufgrund der unterschiedlichen
Spaltausbildungen entlang der Kontur varriert. Wenn die Werkstückgeometrie nur
flache Konturen aufweist, kann jedoch auch schon die verhältnismäßig einfache
Korrektur um einen allseitig konstanten Betrag zur Erzielung einer
vergleichs-weise guten Genauigkeit ausreichend sein. Wie aus obigem Bild
entnommen werden kann, verringert sich die Spaltaufweitung um so mehr, je
größer man die Vorschubgeschwindigkeit wählt. Bei komplizierteren Geometrien
besteht jedoch bis heute nur die Möglichkeit, die Werkzeugkontur durch Versuche
so lange zu berichtigen, bis eine ausreichende Genauigkeit erreicht ist. Das
Verfahren ist sehr zeitaufwendig und macht die Raumformbearbeitung oft
unwirtschaftlich.
Bei Verwendung von passivierenden Elektrolytsystemen laufen die
abtragunwirksamen Reaktionen bevorzugt in unteren Stromdichtebereichen ab.
Entsprechend dem zwischen der Spaltweite s und Stromdichte J bestehenden
Zusammenhang  wird aber damit im
Bereich großer Arbeitsspalte - wie sie bei der Herstellung von Raumformen im
Normal- und Seitenspaltbereich vor-liegen - der Wirkungsgrad der
Metallauflösung verringert. Diese Tatsache bewirkt den erwünschten Effekt der
Begrenzung der Spalaufweitung, da ein Abtrag nur dann stattfinden kann, wenn
eine bestimmte Mindeststromdichte Jmin überschritten ist. Die
Verwendung passivierender Elektrolytlösungen gewinnt insbesondere bei der
Herstellung steiler Raumformen entscheidende Bedeutung, da die durch den
elektrochemischen Porzeß begrenzte Spaltaufweitung eine nahezu konstante
Spaltausbildung auch bei steilen Konturen gewährleistet.
wird aber damit im
Bereich großer Arbeitsspalte - wie sie bei der Herstellung von Raumformen im
Normal- und Seitenspaltbereich vor-liegen - der Wirkungsgrad der
Metallauflösung verringert. Diese Tatsache bewirkt den erwünschten Effekt der
Begrenzung der Spalaufweitung, da ein Abtrag nur dann stattfinden kann, wenn
eine bestimmte Mindeststromdichte Jmin überschritten ist. Die
Verwendung passivierender Elektrolytlösungen gewinnt insbesondere bei der
Herstellung steiler Raumformen entscheidende Bedeutung, da die durch den
elektrochemischen Porzeß begrenzte Spaltaufweitung eine nahezu konstante
Spaltausbildung auch bei steilen Konturen gewährleistet.
Im Hinblcik auf die Formgenauigkeit lassen sich aus dem vA-J-Diagramm
(siehe unten) weitere nützliche Erkenntnisse zur Erzielung eines gewünschten
Arbeits-ergebnisses herleiten. Wird die Vorschubgeschwindigkeit vf
so gewählt, daß der kleinste Spalt nahezu so groß wird wie der größtmögliche
Spalt, ist eine nahezu konstante Spaltausbildung erreichbar. Der Unterschied
der Spaltweiten wird dabei um so kleiner, je langsamer man die
Vorschubgeschwindigkeit wählt. Durch Verringern der Konzentration und Erhähen
der Temperatur kann der Passivier-ungsgrad, der durch die Mindeststromdichte
Jmin charkaterisert wird, so sehr erhöht werden, daß sich eine konstante
Spaltausbildung auch bei höheren Vorschubgeschwindigkeiten erzielen läßt.
Eletkrochemisches Polieren
Verunreinigunen aus der Fertigung befinden sich nicht nur auf den Oberflächen
der Werkstücke, sondern auch in den unmittelbar darunter liegenden
Werkstoff-schichten. Werkzeugabrieb, Zunder, Öle, Fette sowie Reste von
Schleif- und Poliermitteln werden durch die mechanische Bearbeitung in die
Oberfläche eingetragen und anschließend durch überlappendes und verzogenes
Metall zugedeckt, so daß sie allen "oberflächlichen"Reinigungsprozessen widerstehen
und somit zu Störungen im weiteren Arbeitsablauf führen. Zuverlässige Abhilfe
ermöglicht nur die vollständige Beseitgung der verunreinigten
Werkstoffschichten, ohne daß dabei neuerlich Fremstoffe eingeschleppt oder die
Oberflächen anderweitig, etwa durch Korngrenzenangriff geschädigt werden. Dies
ist technisch und wirtschaftlich gleichermaßen befriedigend durch
Elektropolieren möglich. Die oberflächennahen Werkstoffschichten werden dabei
ohne mechanishce und thermische Belastung auf elektrochemischem Wege
abgetragen.
Eine hohe Reinheit wird in der Praxis insbesondere für Bauteile von
kerntechnischen Anlagen sowie für Triebwerksteile für Luft- und Raumfahrt
gefordert. Ein weiteres Anwendungsgebiet dieses Abtragverfahren ist das
Einebnen von Oberflächenrauhigkeiten zur Verminderung von Reibungsprozessen bei
Zahnrädern, Wellen usw.
Elektrochemisches Atzen
Da die Bindungskräfte zwischen den Atomen an der Oberfläche des Metallgitters
von der Sturktur und der Orientierung des Kristalls abhängen und an Fehlstellen,
Versetzungen oder Korngrenzen kleiner sind als im Innern des Kristalls, sind
zur Ablösung eines Metallions aus dem Gitterverban unterschiedliche
Energieschwellen auf der Metalloberfläche zu überwinden. Der Stromfluß entsteht
daher auf Grund von Potentialdifferenzen im Mikrobereich, die einen
elektrochemischen Abtrag mit ungleichmäßiger Verteilung auf der
Metalloberfläche bewirken. Diese Tatsache wird bekanntlich bei der
elektrochemischen Atzung in der Metallographie zum Sichtbarmachen der Gefügestruktur
genutzt.
Zur Anwendung kommen alkalische, saure oder neutrale Atzlösungen, und zwar in
Abhängigkeit von den elektrochemischen Eigenschaften des ätzenden
Werkstückwerkstoffs; gegebenfalls sind auch Mischungen anwendbar. In der Praxis
verwendet man beim Atzen gedruckter Schaltungen vorwiegend neutrale
Atzlösungen.
Die Abtraggeschwindigkeit liegt je nach Werkstoff und Atzbedingugnzwischen 0,01
und 0,08 mm/min. Wesentlich wird sie von der "Badtemperatur" beeinflußt. Mit
steigender Temperatur nimmt die Abtragggeschwindigkeit zu. Um einen
gleichmäßigen Abtrag zu erzielen, muß der Werkstoff in Zusammensetzung und
Gefüge homogen sein. Vielfach müssen daher die Werkstücke vor dem Atzen einer
Wärmebehandlung unterzogen werden.
Die Oberflächengüten geätzter Flächen werden außer von der Atztiefe und dem
verwendeten Atzmedium wesentlich von der chemischen Lälichkeit der einzuelnen
Werkstoffbestandteile, ihrer Konrgrößen und ihrem Anteil am Gesamtwerkstoff
bestimmt. Auch die Ausgangsrauheit ist von Einfluß. Bearbeiteungsspuren,
Riefen, Kratzer und andere Unregelmäßigkeiten isind auf der geätzten Fläche
mehr oder minder "verwaschen" zu sehen. Eine gute Ausgangsrauheit
vorausgesetzt, werden im allgemeinen Rauhtiefen zwischen 1 und 15 mm erreicht.
Im Hinblick auf die erzielbare Abtraggeschwindigkeit - Atztiefe bezogen auf die
Wirkzeit - und der sich daraus ergebende Oberflächengüte werden
unterschiedliche Atzverfahren angewendet. so ist in dem Bild unten außer dem
eigentlichen Abtragprinzip das sogenannte Tauchätzen und das Sprühätzen
schematisch wiedergegeben.
Beim Tauchätzen werden die zu ätzenden werkstücke in eine Wanne mit Atzmittel
eingetaucht. Die Luft- und Raumfahrtindustrie bietet vor allem große
Einsatzmög-lichkeiten, bei denen mit Hilfe dieses Verfahrens die Masse
großflächiger, dünn-wandiger oder räumlcih komplizierter Bauteile verringert
wird, wenn dies mit herkömmlichen Verfahren nicht oder nur in Verbindung mit
einem hohen Kosten-aufwand zu erzielen wäre. Ein wesentlicher Nachteil des
Tauchätzens besteht in der Schwierigkeit, die Reaktionsprodukte von der
Metalloberfläche zu entfernen und das durch die Reaktionswärme aufgeheizte und
mit Gasblasen versetzte Atzmedium in der Nähe der Werkstücke durch frische Flüssigkeit
zu ersetzen.
Beim Sprühätzen wird das Atzmedium durch Düsen mit Druck auf das meist
horizontal angeordnete Werkstück gesprüht und somit die Werkstückfläche
gleichmäßig benetzt. Der Flüssigkeitsdruck spült die Reaktionsprodukte von der
Metalloberfläche.
Die Atztemperatur ist leicht konstant zu halten, da nur kleine Mengen der
Atzlösung erforderlich sind. Zusätzlich ist von Vorteil, daß der gerichtete
Strahl des Atzmediums den Abtragfortschritt senkrecht zur Oberfläche fördert,
so daß eine kleinere Unterätzung auftritt als beim Tazuchätzen. Nachteilig sind
die komplizierten und teuren maschinellen Einrichtungen. Darüber hinaus sind
widerstandsfähigere Abdeckstoffe erforderlich, die von der mit Druck
aufgesprühten Atzlösung nicht unterspült werden.
Die mit Hilfe der Atzverfahren erzielbare Formerzeugung wird durch Abdeckmasken
un zeitlich gestuertes Eintauchen oder Herausziehen des Werkstücks aus dem
Atzmedium ermöglicht. Als Abdeckschichten kommen feste, pastöse und flüssige
Stoffe in Betracht. Als feste bzw. pastöse Abdeckschten werden Kunststoffolien,
Wachse oder pechartige Sotffe, als flüssige Abdeckschcihten Lacke oder flüssige
Kunststoffe verwendet.
Zum Abdecken und Maskieren etnwickelte man eine Reihe von Maskiertechniken. Ein
im großen Umfang angewendetes Verfahren besteht darin, ätzbeständige Streifen
oder vollständig vorgefertigte Abdeckmasken oder Abdeckschablonen auf dem
Werkstück anzubringen. Bei hohen Stückzahlen und komplizierten Konturen werden
die Abdeckungen auf photographischem Wege aufgebracht. Eine andere
Maskiertechnik ist das Siebdruckverfahren.